感染症と対策
新型インフルエンザウイルスのパンデミックや肝炎訴訟、あるいは、SARSの流行やエボラ出血熱、エイズ等のウイルスに起因する感染症の解決は、社会的に非常に重要な課題です。ウイルスがヒトに感染すると、ヒトは自然免疫と獲得免疫で身を守ります。B細胞やT細胞等のリンパ球から構成される獲得免疫は、一度感染したウイルスに二度と感染しないために非常に重要です。一方の自然免疫は、感染初期や、初めて感染するウイルスに対して身を守るために特に重要な働きをします。また、最近の研究から、自然免疫は獲得免疫の活性化にも重要な働きをすることが解明されてきました。ウイルスに感染した場合の自然免疫応答としてヒトの細胞から産生されるI型インターフェロンは、強い抗ウイルス作用を持ち、C型肝炎の治療薬としても用いられています。このことからも、自然免疫の重要性が理解できます。
このように、ヒトの自然免疫はウイルスを排除します。では、なぜ、ウイルスはヒトに感染できるのでしょうか? 実は、ウイルスは、この自然免疫を抑制することで、ヒトに感染できるのです。しかし、ウイルスが自然免疫を抑制する仕組みについてはまだ十分に解明されていません。つまり、このウイルスに対する自然免疫応答と、ウイルスが自然免疫応答を抑制する仕組みを解明することは、ウイルス感染症に対する新たな治療薬や治療法の開発の一つの鍵になると期待されます。そこで、私たちはこれまで、ウイルスに対する自然免疫応答の仕組みと、ウイルスがこの自然免疫応答を抑制する仕組みの解明にこれまで取り組んできました。
C型肝炎ウイルス(Hepatitis C virus: HCV)
C型肝炎ウイルスはヒトの肝癌のおよそ70%の原因として知られています。また、日本では現在数百万人の感染者がいると考えられています。これまでのHCV感染患者に対する治療薬として、ペグインターフェロンとリバビリンの併用療法が用いられてきましたが、日本人患者に多い型のウイルス感染に対しては、この併用療法の効果が高くないことや、インターフェロンによる副作用の問題等がありました。最近承認された、テラプレビルも、高齢者への副作用の問題や、薬が高価であるための経済的な負担の問題があります。
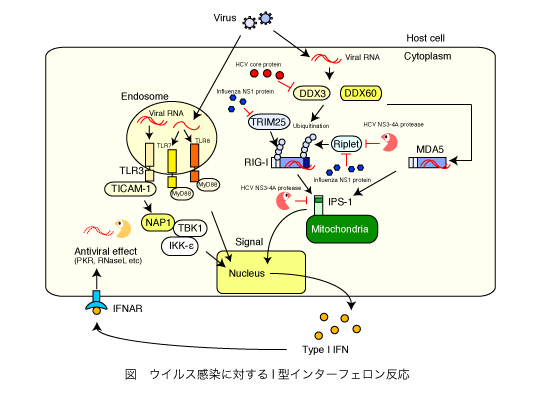
我々はC型肝炎ウイルス感染症に対する基礎研究として、まずHCV感染時の自然免疫応答機構の研究を行っています。これまでの研究から、HCV感染時には樹状細胞のエンドソーム内に存在するTLR3と呼ばれる受容体が、HCVに感染した肝細胞からHCVのRNAを受け取り、自然免疫応答を引き起こすことを発見しました(16)。またHCV感染時にはIPS-1(MAVS)分子を介してIII型インターフェロンが産生されることを発見しました(1)。このIII型インターフェロンの遺伝子配列のわずかな違いがHCV感染患者の治療成績と非常に関連が高いことが知られています。また、細胞質内のウイルス認識センサーのRIG-Iの活性化に必要な分子として、これまでRipletと名付けた分子や(11, 14)、DDX3やDDX60として知られていた分子が重要であることも発見しました(8, 13)。
一方で、HCVが自然免疫を抑制する仕組みとして、HCVのコアタンパク質が上記のDDX3分子の活性を抑制することや(12)、HCVのプロテアーゼが上記のRiplet分子を切断することで、I型インターフェロンの産生を抑制することなども解明しました(5)。このことから、今後、HCVによるDDX3やRiplet分子の抑制を解除する薬剤の発見や開発が、C型肝炎患者に対する新たな治療薬や治療法の開発に繋
がると期待されます。
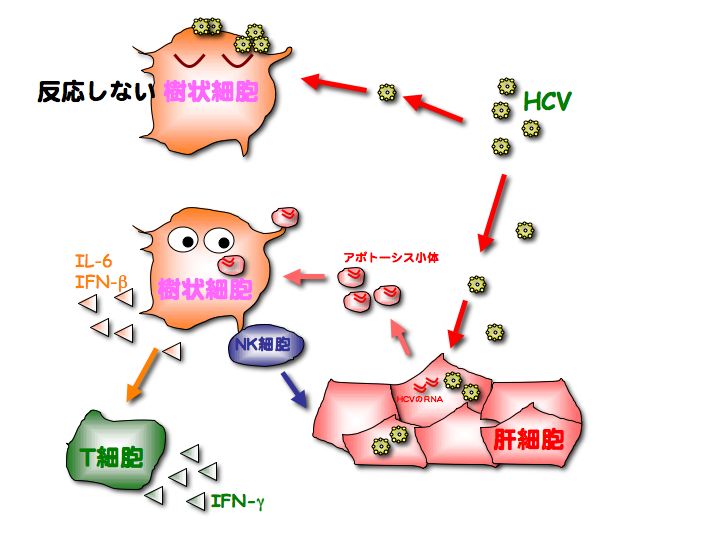
図 HCV感染によるアポトーシスを介した樹状細胞の活性化
麻疹ウイルス(Measles virus: MV)
麻疹ウイルスはパラミクソウイルス科に属する-鎖のRNAをゲノムに持つウイルスです。私たちは、古くから研究に用いられてきたMVの株では欠損干渉粒子(Defective interfering particle:DI粒子)が含まれ、これが抗ウイルス作用をもつI型インターフェロンの産生を誘導することを発見しました(18)。現在、私たちは、このDI粒子を感染症や癌の治療に用いる為に研究を進めています。
麻疹ウイルスはヒトを含む霊長類以外の動物には感染しません。そこで、私たちは麻疹ウイルスが、ヒト細胞に感染するときの足場となるヒトのCD46(MCP)分子とCD150 (SLAM)分子の遺伝子をマウスに導入した遺伝子改変マウスを作製しました(20)。このマウスを用いた解析から、麻疹ウイルスの感染成立にはCD11c陽性の樹状細胞が重要であることや(20)、麻疹ウイルス感染時のI型インターフェロン産生経路として、CD4陽性の樹状細胞や形質細胞様樹状細胞のMyD88分子が関与する経路が重要であること(4)、骨髄由来樹状細胞ではIPS-1(MAVS)分子がMV感染の抑制に重要であること(3)を発見しました。このIPS-1分子は麻疹ウイルス感染時にはMDA5と呼ばれる分子からシグナルを受けてI型インターフェロン産生を誘導しますが、我々は、麻疹ウイルスのVタンパク質のアミノ酸配列が、麻疹ウイルスの株によって少し異なり、これが原因で麻疹ウイルス感染時のMDA5活性化の程度がウイルス株の違いで変化することを解明しました(10)。

図 麻疹感染モデルマウス
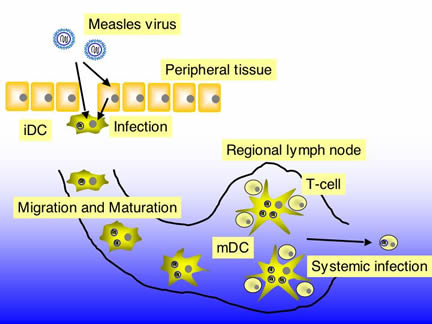
図 麻疹ウイルスの樹状細胞を介した全身感染
説明:体内に侵入した麻疹ウイルスは、まず未成熟な樹状細胞(iDC)へと感染 します。局所にて感染した樹状細胞は、抗原を取り込んだ樹状細胞と同じく、成熟化しながら(成熟樹状細胞mDC) リンパ管を通り、局所リンパ節へ抗原を提示するために遊走します。局所リンパ節で、成熟樹状細胞は抗原を 提示するためTリンパ球と接触します。このようにして麻疹ウイルスはリンパ球へ感染し、全身へと広がります。
その他のウイルス
私たちの研究室では上記のHCVとMVだけでなく、ポリオウイルスやB型肝炎ウイルス、単純ヘルペスI型ウイルス等も研究しています。ポリオウイルスは、ヒトの小児麻痺の原因として知られており、現在、世界的にポリオ撲滅のための活動が実施されています。私たちはポリオウイルス感染のマウス動物モデルを用いて、このポリオウイルス感染時には、私たちが発見したTICAM-1分子が非常に重要な働きをすることをこれまでに発見しました(6, 7)。
B型肝炎ウイルスや単純ヘルペスI型ウイルスは、DNAをゲノムに持つウイルスですが、ウイルスのDNAによって生じる自然免疫機構はまだ十分に解明されていません。私たちは、このウイルスのDNAによって生じる自然免疫機構の研究をしたところ、ヒトの細胞とマウスの細胞では、この自然免疫機構が異なることを発見しました(2)。
今後は、これらの発見を基礎として、臨床に繋がる研究も発展させていく予定です。
発表論文
- Okamoto M, Oshiumi H, Azuma M, Kato N, Matsumoto M, Seya T. 2014. IPS-1 is essential for type III interferon production by hepatocytes and dendritic cells in response to hepatitis C virus infection. J. Immunol. in press.
- Suzuki T, Oshiumi H, Miyashita M, Aly HH, Matsumoto M, Seya T.2013. Cell Type-Specific Subcellular Localization of Phospho-TBK1 in Response to Cytoplasmic Viral DNA. PLoS One. 8(12):e83639.
- Takaki H, Honda K, Atarashi K, Kobayashi F, Ebihara T, Oshiumi H, Matsumoto M, Shingai M, Seya T.2014. MAVS-dependent IRF3/7 bypass of interferon β-induction restricts the response to measles infection in CD150Tg mouse bone marrow-derived dendritic cells. Mol Immunol. 57(2):100-110.
- Takaki H, Takeda M, Tahara M, Shingai M, Oshiumi H, Matsumoto M, Seya T. 2013. The MyD88 pathway in plasmacytoid and CD4+ dendritic cells primarily triggers type I IFN production against measles virus in a mouse infection model. J Immunol. 191(9):4740-4747.
- Oshiumi H, Miyashita M, Matsumoto M, and Seya T. 2013. A Distinct Role of Riplet-Mediated K63-Linked Polyubiquitination of the RIG-I Repressor Domain in Human Antiviral Innate Immune Responses. PLos Pathogens 9(8), e1003533.
- Abe Y, Fujii K, Nagata N, Takeuchi O, Akira S, Oshiumi H, Matsumoto M, Seya T, Koike S. 2012. The toll-like receptor 3-mediated antiviral response is important for protection against poliovirus infection in poliovirus receptor transgenic mice. J Virol. 86(1):185-94.(IF=5.076, CI=5)
- Oshiumi H, Okamoto M, Fujii K, Kawanishi , Matsumoto M, Koike S, and Seya T. 2011. The TLR3-TICAM-1 pathway is mandatory for innate immune responses to poliovirus infection J. Immunol 187(10):5320-7.
- Miyashita M, Oshiumi H, Matsumoto M, and Seya T. 2011. DDX60, a DExD/H box helicase, is a novel antiviral factor promoting RIG-I-like receptor mediated signaing Mol. Cell. Biol. 31: 3802-3819.
- Aly HH, Oshiumi H, Shime H, Matsumoto M, Wakita T, Shimotohno K, Seya T.2011. Development of mouse hepatocyte lines permissive for hepatitis C virus (HCV). PLoS One. 6(6):e21284.
- Takaki H, Watanabe Y, Shingai M, Oshiumi H, Matsumoto M, Seya T.2011. Strain-to-strain difference of V protein of measles virus affects MDA5-mediated IFN-β-inducing potential. Mol Immunol. 48(4):497-504.
- Oshiumi H#, Miyashita M, Inoue N, Okabe M, Matsumoto M, and Seya T. 2010. The ubiquitin ligase Riplet is essential for RIG-I-dependent innate immune responses to RNA virus infection. Cell Host & Microbe 8: 496-509.
- Oshiumi H, Ikeda M, Matsumoto M, Watanabe A, Takeuci O, Akira S, Kato N, Shimotohno K, Seyat T. 2010. Hepatitis C virus core protein abrogates the DDX3 function that enhances IPS-1-mediated IFN-beta induction. PLos One 5(12): e14258.
- Oshiumi H, Sakai K, Matsumoto M, Seya T.2010. DEAD/H BOX 3 (DDX3) helicase binds the RIG-I adaptor IPS-1 to up-regulate IFN-beta-inducing potential. Eur J Immunol. 40(4):940-948.
- Oshiumi H, Matsumoto M, Hatakeyama S, Seya T. 2009. Riplet/RNF135, a RING finger protein, ubiquitinates RIG-I to promote interferon-beta induction during the early phase of viral infection. J Biol Chem. 284(2):807-817.
- Matsuo A, Oshiumi H, Tsujita T, Mitani H, Kasai H, Yoshimizu M, Matsumoto M, Seya T. 2008. Teleost TLR22 recognizes RNA duplex to induce IFN and protect cells from birnaviruses. J Immunol. 181(5):3474-3485.
- Ebihara T., M. Shingai, M. Matsumoto, T. Wakita, T. Seya. 2008. Hepatitis C virus-infected hepatocytes extrinsically modulate dendritic cell maturation to activate T cells and natural killer cells. Hepatology 48(1)48-58.
- Shingai M., M. Azuma, T. Ebihara, M. Sasai, K. Funami, M. Ayata, H. Ogura, H. Tsutsumi, M. Matsumoto, T. Seya. 2008. Soluble G protein of respiratory syncytial virus inhibits Toll-like receptor 3/4-mediated IFN-beta induction. Int. Immunol. 20(19):1169-1180.
- Shingai, M., T. Ebihara, N. A. Begum, A. Kato, , T. Honma, K. Matsumoto, H. Saito, H. Ogura, M. Matsumoto, and T Seya. 2007. Defective interference RNA participates in type I interferon induction and maturation of human dendritic cells. J. Immunol. 179(9):6123-6133.
- Ebihara, T., H. Masuda, T. Akazawa, M. Shingai, H. Kikuta, T. Ariga, M. Matsumoto, and T. Seya. 2007. NKG2D ligands are induced on human dendritic cells by TLR ligand stimulation and RNA virus infection. Int. Immunol. 19(10):1145-1155.
- Shingai, M., N. Inoue, M. Okabe, T. Akazawa, Y. Miyamoto, M. Ayata, K. Honda, M. Kurita- Taniguchi, M. Matsumoto, H. Ogura, T. Taniguchi, and T. Seya. 2005. A mouse model for wild-type measles virus infection: CD11c-positive dendritic cells are nidus for systemic viral spreading. J. Immunol. 175: 3252-3261.
- Tanabe, M., M. Kurita-Taniguchi, K. Takeuchi, K. Funami, M. Matsumoto, M. Shingai, M. Ayata, H. Ogura, and T. Seya.2003. Mechanism of up-regulation of human Toll-like receptor 3 secondary to infection of measles virus-attenuated strains. Biochem. Biophys. Res. Commun. 311: 39-48.
- Murabayashi, N., M. Kurita-Taniguchi, M. Ayata, H. Ogura, M. Matsumoto, and T. Seya. 2002. Susceptibility of human dendritic cells to measles virus depends on their activation stages in conjunction with the level of CDw150: role of Toll stimulators in DC maturation and MV amplification.Microbes Infect. 4: 785-794.
- Nishiguchi, M., M. Matsumoto, T. Takao, M. Hoshino, Y. Shimonishi, S. Tsuji, O. Takeuchi, S. Akira, K. Toyoshima, and T. Seya. 2001. Mycoplasma fermentans lipoprotein M161Ag-induced cell activation is mediated by Toll-like receptor 2: Role of N-terminal hydrophobic portion in its multiple functions. J. Immunol. 166: 2610-2616.
- Moriwaki, Y., N. A. Begum, M. Kobayashi, S. Tsuji, M. Nomura, M. Matsumoto, K. Toyoshima, and T. Seya. 2001. Mycobacterium bovis Bacillus Calmette-Guerin and its cell wall complex induce a novel lysosomal membrane protein, SIMPLE, that bridges the missing link between lipopolysaccharide and p53-inducible gene, LITAF (PIG7), and estrogen-inducible gene, EET-1. J. Biol. Chem. 276: 23065-23076.
- Tsuji, S., M. Matsumoto, O. Takeuchi, S. Akira, I. Azuma, A. Hayashi, K. Toyoshima, and T. Seya. 2000. Maturation of human human dendritic cells by cell-wall skeleton of Mycobacterium bovis Bacillus Calmette-Guerin: involvement of Toll-like receptors. Infect. Immun. 68: 6883-6890.
- 瀬谷司、新開大史、松本美佐子、Toll—like receptor(TLR)と抗ウイルス応答、ウイルス. ウイルス学会誌 54(1):1-8, 2004.
- 新開大史、松本美佐子、瀬谷司、異種間ウイルス伝搬における自然免疫の役割、臨床ウイルス 臨床ウイルス 学会 35: 21-29, 2007.