自然免疫から見た抗がん免疫(阪大学友会, 2009)
北海道大学大学院医学研究科 免疫学分野 瀬谷 司
これまで○×に対する免疫、と云えば○×は微生物であり抗原の提供者であった。ワクチンは抗原が アプリオリの人為的な免疫源を意味してきた。免疫の起動にアジュバント(adjuvant)を用いることは 古くから行われ、Freund complete adjuvant (FCA), 水酸化アルミニウム(alum)、などを抗原とconjugate して頻用されてきた。これらの作用機序は最近まで明らかでなく、抗原を“汚す”ことで免疫能を高める、 という解釈であった。
自然免疫のレセプター、特にToll-like receptor (TLR), の機能研究とアゴニスト検索からadjuvant の成分はTLRなどのagonist(パターン分子, PAMP)であることが判明し、免疫系に指向性を付与する原基 は自然免疫(樹状細胞とパターン認識)であるという修正がなされている (1)。即ち抗原は免疫の対象を 決めるだけで戦略は決めない。戦略とは抗体、NK, CTL, Th17, Treg などのエフェクターである(図1)。 がんは抗原があるがパターン分子を欠く典型例であり、ワクチンの有効性が戦略に依存するのは当然である。 がん抗原は対象を決めるがエフェクター誘導までは指示しない。それを決めるのはアジュバントである (2)。
このような起草は私のオリジナルではないと思う。旧くから明晰の先達はおられた。但し、その時代に その考え方が受理されなかっただけである。発想は時代の必然性によって発展する。現在このような考え方 がフィットする理由はPAMP識別のレセプターが複数あって異なった炎症応答を惹起することが見通せるから である。
PAMPのレセプターとはパターン認識レセプターのことで、TLRはその代表である。パターン認識レセプタ ーは複数あって異なったアダプターが多様な樹状細胞成熟化を誘導する。結果として別個のエフェクターを ドライブする。重要なアダプターとしてTLR3, 4のTICAM-1 (TRIF), TLR3以外のMyD88, RIG-I/MDA5 のIPS-1 (MAVS, Cardif, VISA), Nod-like receptor のASCがある。私たちのグループはTLR3/TICAM-1 経路の同定に 関わった(3)。
パターン認識レセプターは微生物のセンサーであり、細胞種、細胞内局在、PAMPの種類などによって使い 分けられる。核酸のPAMPを例にとると細胞質で増えるRNAウイルスと核内で複製するRNAウイルス(Borna, Influenza)は自ずと異なる宿主識別レセプターとシグナルアウトプットをとって当然である。DNAウイルス でも細胞質封入体を作って増えるものがある。しかし、多くのDNAウイルスは核内で複製し、TLR9を使わない。 一方でがん抗原は外から取り込まれて樹状細胞に入る。同様の経路でPAMPが取り込まれた場合の免疫応答は 樹状細胞の細胞質でなく貪食(食胞?endosome)で起きる。Endosome にはTLR3が発現しており、抗原とRNAが conjugate しておれば強い抗原特異免疫が起動するはずである (4)。私たちはこのような発想から副作用の 少ないRNAアジュバントの開発を目指している (5)。
私たちの研究ルーツは大阪にある。大阪府立成人病センターは研究所を有するがんの高度先進医療機関で ある。私は16年間研究所に在籍した。1994年に豊島久真男先生が総長として赴任し、研究所は 2001 年から 文科省認可となった。科研費の申請が出せることに感激した。病院と研究所は大学では想像もつかぬ程交流 が容易で豊島先生はがんのBCG-CWS免疫療法をそのような基盤の上に立ち上げられた。炯眼というべきである。 BCG-CWSはTLR2/4のアゴニストであり(6)、これは将にアジュバント療法であった。成果は児玉憲副院長の 論文に見る様に(7)、恐らく(ランダマイズドではないが)抗原単独療法(8)より優る。BCG-CWSはペプチ ドグリカン構造を活性中心に持ち、合成が不可能であった。生物製剤の創薬化という難しさがあり、その後 それ以上のアジュバントを合成し、探索する試金石になった。
感染を理解する基礎研究がアジュバントの機能査定には必須である。大阪は微研と公衛研、武田の発酵研 を擁するため、極めて有利な地の利をもつことが分かった。多くの微生物成分の特徴が知識と材料で支えられ ていた。それを支える人材の素晴らしさと層の厚さも大変ありがたかった。ただし、この時期、公衛研は府の 財政難から改組され、研究陣は縮小した。私も所長業務の傍らで「府民の税金を研究に使って何の役に立つん や」という議員の言葉を何度も聞いた。微研でも惜しいことに感染とがんを互換的に理解しうる人材は特にが んの側からは衰退していた。
阪大微研が感染症と免疫に特化を目指すのも時代の反映で、私はその可否を論じる立場には無い。しかし、 がん研究もウイルスと免疫の申し子である。オンコジーンの時代があり、がん特異抗原の時代があった。旧い 微研ジャーナルは研究に人生をかけた人々の足跡をたどる温故知新の旅でもある。いつの時代も研究は順風満 帆の環境で進められるものではない。変転する社会状勢と世相の中でそれでも飽くなき真理の探究を目指した 人々のヒストリーである。日本は急速な近代化を遂げたが欧米の雑誌を規範として欧米の価値観で自国の研究 史を刷新した。母国語でなく不慣れな外国語でニーズを主張することのどこに国際化があるのか。自国軽視の 歪みは必ずしも勝利者とはならず引用されなくなった過去の論文に投影される。私はNature でなくともその ような論文を心から顕彰するものである。
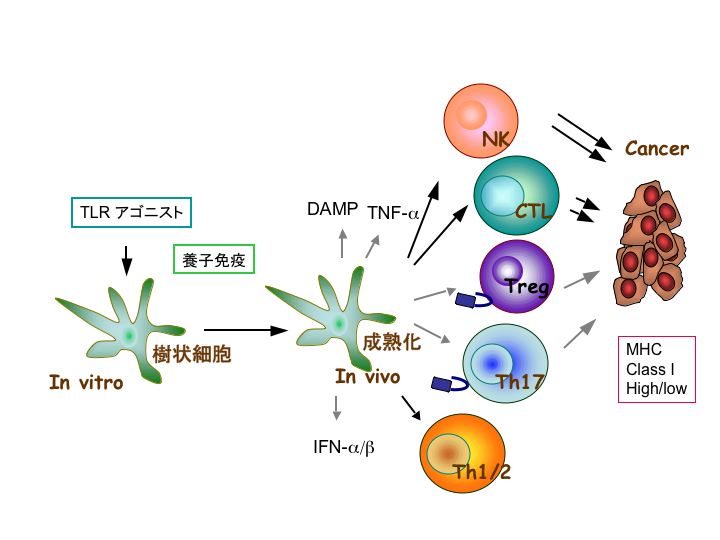
図1
図1の説明
各種TLRアゴニスト(PAMP)は多様な樹状細胞成熟化を誘導し、異なったエフェクター細胞をドライブ
する。樹状細胞のTLR下流のアダプター分子が転写因子を活性化してNKやCTL 誘導を指定する。それらを
実行する分子を樹状細胞内に発現させる。PAMPで刺激した樹状細胞をがんの周囲に養子免疫するとエフェ
クターの査定ができる。
文献
- Iwasaki A, Medzhitov R. Toll-like receptor control of the adaptive immune responses. Nat Immunol. 5(10):987-995, 2004.
- Seya T., Oshiumi H., Matsumoto M, Pattern recognition receptors and their application to tumor immunotherapy. Cancer Sci. (review) in press.
- Oshiumi H, Matsumoto M, Funami K, et al. TICAM-1, an adaptor molecule that participates in Toll-like receptor 3-mediated interferon-beta induction. Nat Immunol. 4(2):161-167, 2003.
- Matsumoto M, Seya T. TLR3: interferon induction by double-stranded RNA including poly(I:C). Adv Drug Deliv Rev. 60(7):805-812, 2008.
- Seya T, Matsumoto M. The extrinsic RNA-sensing pathway for adjuvant immunotherapy for cancer. Cancer Immunol. Immunother. 58(2):1175-1184, 2009.
- Tsuji S, Matsumoto M, Takeuchi O, et al. Maturation of human dendritic cells by cell wall skeleton of Mycobacterium bovis bacillus Calmette-Gu?rin: involvement of toll-like receptors. Infect Immun. 68(12):6883-6890, 2000.
- Kodama K, Higashiyama M, Takami K, et al. Innate immune therapy with a Bacillus Calmette-Gu?rin cell wall skeleton after radical surgery for non-small cell lung cancer: a case-control study. Surg Today. 39(3):194-200, 2009.
- Rosenberg SA, Yang JC, Restifo NP. Cancer immunotherapy: moving beyond current vaccines. Nat Med. 10(9):909-915, 2004.